El universo vuelve a sorprendernos con un fenómeno meteorológico tan familiar como extraño: un planeta gigante fuera del sistema solar parece tener mañanas cubiertas de nubes y tardes despejadas. La diferencia es que allí no hablamos de brisas suaves ni de lluvias pasajeras, sino de temperaturas extremas y vientos supersónicos en un mundo gaseoso abrasado por su estrella.
El descubrimiento, publicado en la revista Science y realizado con el telescopio James Webb (JWST), aporta una de las imágenes más detalladas hasta ahora de cómo funcionan las atmósferas de los exoplanetas gigantes. Y, además, ayuda a resolver un viejo debate de la astronomía moderna: ¿de qué están hechas realmente las neblinas (hazes) y nubes que envuelven estos mundos?

Un “Júpiter caliente” con dos caras

El protagonista del estudio es WASP-94A b, un “Júpiter caliente”: un planeta gaseoso parecido a Júpiter, pero orbitando extremadamente cerca de su estrella. Esa proximidad hace que un año allí dure apenas unos días terrestres y que el planeta esté acoplado de marea, es
decir, mostrando siempre la misma cara a su sol.
Como ocurre con la Luna respecto a la Tierra, un hemisferio permanece eternamente iluminado y el otro en oscuridad constante. Entre ambos, existe una franja de transición, llamada “terminador”, donde los astrónomos pueden estudiar la atmósfera observando cómo la luz de la estrella atraviesa sus capas gaseosas durante un tránsito planetario.

Y fue precisamente allí donde apareció la sorpresa.
Las observaciones del JWST revelaron una diferencia muy clara entre el lado matutino y el vespertino del planeta. En la región donde amanece, predominan densas nubes que amortiguan las señales espectrales del vapor de agua. En cambio, en la zona donde anochece, la atmósfera aparece mucho más limpia y transparente.
El ciclo meteorológico más extremo imaginable
La explicación apunta a un auténtico ciclo meteorológico extraterrestre. Los investigadores creen que las nubes se forman en las regiones relativamente más frías del planeta, probablemente mediante condensación de minerales y compuestos exóticos presentes en la atmósfera. Después, los potentes vientos atmosféricos transportan esas partículas hacia zonas más calientes, donde terminan evaporándose.
En la Tierra, las nubes están formadas por agua líquida o cristales de hielo. Pero en estos mundos abrasadores, podrían existir nubes de silicatos o minerales vaporizados. Las diferencias térmicas entre ambos lados del planeta pueden superar los 280 grados centígrados, suficientes para que los aerosoles aparezcan y desaparezcan continuamente mientras circulan alrededor del globo.

Los nuevos datos del JWST sugieren, además, que la distribución de las nubes no es uniforme ni estable. Las observaciones indican una atmósfera extremadamente dinámica, dominada por corrientes capaces de redistribuir calor y materiales a velocidades enormes.
En este escenario, los modelos atmosféricos apuntan a vientos supersónicos que recorrerían el planeta transportando partículas condensadas desde el hemisferio nocturno y las regiones matutinas hacia zonas progresivamente más calientes.
¿Un viejo dilema resuelto?
El hallazgo es importante porque durante años existieron dos hipótesis principales para explicar los aerosoles de los Júpiter calientes. Mientras que una defendía que eran nubes originadas por condensación, la otra proponía neblinas fotoquímicas, creadas por la intensa radiación estelar, similares a las de Titán, la luna de Saturno, o al smog terrestre.
Las nuevas observaciones favorecen claramente la primera explicación: al menos en este tipo de planetas, las nubes parecen comportarse como sistemas meteorológicos dinámicos gobernados por la temperatura y la circulación atmosférica.
El problema de las atmósferas “ocultas”
Aunque las nubes hacen estos mundos más fascinantes, también representan un gran desafío científico.
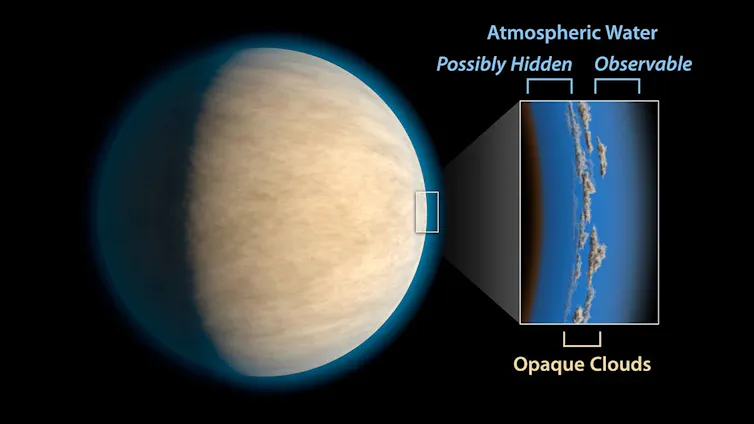
Para estudiar un exoplaneta, los astrónomos analizan cómo ciertos gases absorben longitudes de onda específicas de la luz. Ese patrón permite identificar moléculas como agua, dióxido de carbono o metano. Pero las nubes y neblinas pueden ocultar parte de esas señales y distorsionar las mediciones.
En algunos casos, un planeta puede parecer pobre en agua simplemente porque las nubes bloquean la observación. De hecho, estudios anteriores ya habían mostrado que muchos Júpiter calientes forman un continuo que va desde atmósferas completamente despejadas hasta otras muy cubiertas por nubes.
Ahora sabemos algo aún más complejo: un mismo planeta puede tener regiones simultáneamente nubladas y despejadas.
Esto obliga a reinterpretar parte de los datos obtenidos durante más de una década con telescopios como el Hubble y a desarrollar modelos atmosféricos tridimensionales mucho más sofisticados.
Más cerca de entender otros mundos
El JWST está inaugurando una nueva etapa en la exploración de exoplanetas. Ya no basta con detectar su existencia: ahora empezamos a estudiar su meteorología, sus ciclos atmosféricos y su química con un detalle impensable hace apenas unos años.
WASP-94A b se ha convertido en uno de los mejores ejemplos de esta nueva astronomía atmosférica. Sus “amaneceres” cubiertos de nubes y sus “atardeceres” despejados muestran que incluso los mundos más extremos poseen dinámicas complejas, cambiantes y sorprendentemente parecidas, en ciertos aspectos, a fenómenos meteorológicos familiares en la Tierra.
Comprender cómo se forman estas nubes exóticas también será fundamental para interpretar planetas más pequeños y potencialmente habitables. Después de todo, la atmósfera es la gran intermediaria entre la superficie de un mundo y el espacio.
Por primera vez, comenzamos a observar cómo cambia el tiempo… en planetas situados a cientos de años luz de distancia.


